|
|
|
QQ��:21255156��1801335159(��ױƷ�걨)|915369983(����Ʒע��)|281613376(ͨ��);����:zhuceabc@zhuceabc.com |�Ź��ں����걨����|����ѯ��1801335159(QQͬ��) |
һ���ۼ�����
�ۼ���ԭ�ϡ����Ͼ����顢���Ȼ���Ƴɵĸ����ĩ״��Ʒ��
�����ۼ���Ʒ˵�����й�����
�������ݽ���Էۼ�ʳƷ��̬�涨����Ҫ������й�Ҫ���漰ʹ�õ�ԭ�����Ƴɲ�Ʒʱ����Ҫ���ϵ������涨��
��Ʒ˵�������й�����Ҫ�����£�
��������Ⱥ���ü���Ӧ��������������Ⱥ
����������Ⱥ���ü��������ض��IJ�������Ⱥ
��ʳ������ʳ�÷�����ÿ�����ʳ����Ϊ20g��������ʾ���ۼ�����ʱһ�����ڻ��ɢ��ˮ��������Һ���з��ã�Ҳ��ֱ����ˮ�ͷ���������ʳ�÷���Ϊ��ֱ�ӿڷ����ģ���������ȺӦ������6��������Ⱥ����
������ڴ������װ�ģ���ÿ����װ��װ��������500g��ԭ���ϲ�����1���µķ����������������װӦ���ּ������þߡ�
�������ڡ�������24����
�����ۼ���Ʒ����Ҫ���й�����
�������ݽ���Էۼ�ʳƷ��̬�涨����Ҫ������й�Ҫ���漰ʹ�õ�ԭ�����Ƴɲ�Ʒʱ����Ҫ���ϵ������涨��
��Ʒ����Ҫ���й�����Ҫ�����£�
���й�Ҫ��

������ָ�
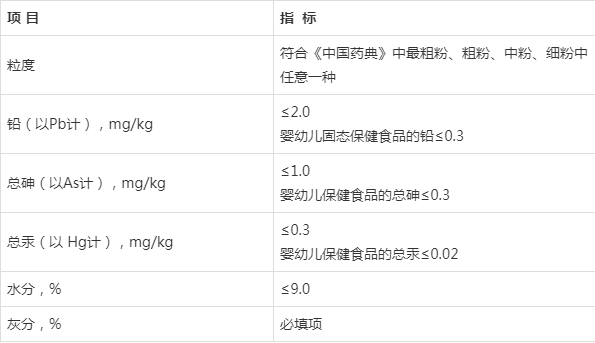
������ָ�
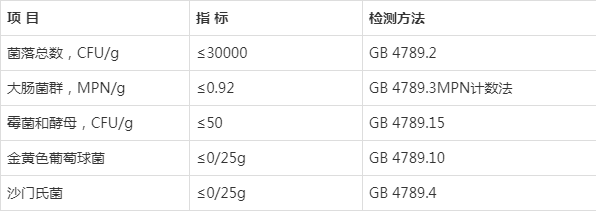
����������������ƫ��ָ�
��������������ƫ��ָ��Ӧ����JJF 1070�涨
�ġ���Ʒ����
�̱���+ͨ����+�ۣ�ԭ�������Ѵ����ۡ��IJ����ظ����ӣ�
�ۼ���Ϊһ��ʳƷ��̬Ŀǰ������800�������ʳƷ��Ϊ���ƽ�����ʳƷ����������������Ʒ����ʳƷ��̬����һ���ƽ�ע��ת����������ʹ�����ʳƷ��̬���뱸���������ܾ�ʳƷ����������֯�ƶ��˱�����Ҫ���ڱ�����Ҫ���ƶ������ж����֯ר�ҽ������֣��������ȡ����ҵЭ���������ҵ�Ľ��飬�����γ��˱�����������塣
һ���ۼ�����
���������е�ʳƷ��ȫ������û�й��ڡ��ۡ���ʳƷ��̬��ר���������ر���Ŀǰ��GB/T 29602-2013���������ϡ����ж��ڹ������ϵĶ���Ϊ����ʳƷԭ���ϡ�ʳƷ���Ӽ��ȼӹ��Ƴɵķ�ĩ״������״���״�ȣ��������������õĹ�̬��Ʒ�������еġ���ĩ״�������������ġ��ۡ��ౣ��ʳƷ������״������ͬ���ڡ��й�ҩ�䡷��2015��棩���IJ����Ƽ�ͨ�����£�ɢ������Ϊ��ָԭ��ҩ��������˵ĸ��Ͼ����顢���Ȼ���Ƴɵĸ����ĩ״�Ƽ��������������ۡ����Ʒ���������պ���״����������ͬ����˱���Ʒ����Ҫ����ƶ���ͬʱ����GB/T 29602-2013���������ϡ��͡��й�ҩ�䡷��2015��棩���й�Ҫ��
�����ۼ���Ʒ˵�����й�����
�������ݽ���Էۼ�ʳƷ��̬�涨����Ҫ������й�Ҫ���漰ʹ�õ�ԭ�����Ƴɲ�Ʒʱ����Ҫ���ϵ������涨��
1. ������Ⱥ�Ͳ�������Ⱥ
�ü���Ӧ��������������Ⱥ��������ʳ�÷���Ϊ��ֱ�ӿڷ����ģ���������ȺӦ������6��������Ⱥ����
2. ʳ����
Ŀǰ�ڡ�����ʳƷ������Ʒ���ø��ϼ���ʹ�ù涨��2019��棩����ʹ��˵����û�����ʳƷ��̬��Ʒ��ÿ�����ʳ�������ʲο�Ŀǰ�����Ƽ���ÿ��ʳ������ֵ��ÿ�����ʳ����������20g����
3. ʳ�÷���
��ʾ���ۼ�����ʱһ�����ڻ��ɢ��ˮ��������Һ���з��ã�Ҳ��ֱ����ˮ�ͷ�����
4. ���
�����Ѿ�������ʳƷ�Ĺ���Լ�����ʳ�õIJ�Ʒ�����ɿ��ԣ������������ΰ�װ�IJ�Ʒ�⣬���ڴ������װ�IJ�Ʒ����ÿ����װ��װ��������500g��ԭ���ϲ�����1���µķ����������������װӦ���ּ������þߡ�
5. ������
����Ŀǰע�ᱣ��ʳƷ�ı������ƶ���ԭ���Լ��ۼ����䷽�����������ص㣬�ۼ��ı����ڲ�Ӧ����24���¡�
�����ۼ���Ʒ����Ҫ���й�����
�������ݽ���Էۼ�ʳƷ��̬�涨����Ҫ������й�Ҫ���漰ʹ�õ�ԭ�����Ƴɲ�Ʒʱ����Ҫ���ϵ������涨��
1. �й�Ҫ��
����Ҫ���ƶ�ʱ�����ɫ����ζ��ζ���趨ʱӦ���ϵľ���Ҫ������Ӧ�ø��ݲ�Ʒ�ľ��������д��
���ڲ�Ʒ״̬�������������Ʒ��Ӧ������ɡ���Ͼ��ȡ�ɫ��һ�¡�
2. ����ָ��
���ȣ�Ϊ���ϸ���Ʊ�����Ʒ��������ͬʱ����ʳƷ��̬�����ڿ�����������ʳƷ��̬����Է����Ʒ�������ԣ�������������������Ҫ����Ҫ���⣬�ο��������������������ƶ���ָ�ꡣ���й�ҩ�䡷�й涨ɢ���ڷ�ʱӦΪϸ�ۣ������ǵ�����ʳƷ����ԭ���ھ��������Һ��������ܽϴ����ﵽ���й�ҩ�䡷��ɢ���ġ�ϸ�ۡ�Ҫ������ڱ������������ȡ�ָ��ʱ�����ա��й�ҩ�䡷�е���ַۡ��ַۡ��зۡ�ϸ�۵ı��������˿���ѡ������һ�ֹ��ġ��ۡ���
Ǧ�����顢�ܹ�ָ�꣺����GB16740-2014��ʳƷ��ȫ���ұ� ����ʳƷ���жԹ����Ƽ���Ҫ������Ǧָ�꣺������Ϊ2.0��Ӥ����̬����ʳƷ��Ǧ����Ϊ0.3����������ָ�꣺������Ϊ1.0��Ӥ������ʳƷ����������Ϊ0.3�������ܹ�ָ�꣬������Ϊ0.3��Ӥ������ʳƷ���ܹ�����Ϊ0.02��
ˮ�֣�GB/T 29602-2013���������ϡ�����ˮ��Ӧ������7.0%�����й�ҩ�䡷��ɢ����ˮ�ֲ��ó���9.0%���ۺ�������������ʳƷ�з����Ʒ��ˮ�ֲ�Ӧ����9.0%��
�ҷ֣������Ƽ�Ӧ���ݲ�Ʒ���ԡ����鱨����ƶ���ָ�ꡣ
3. ����ָ��
����GB16740-2014��ʳƷ��ȫ���ұ� ����ʳƷ���Ĺ涨�������ǹ����ڹ����Ƽ���Ӧ����������йع涨��
4.��������������ƫ��ָ��
����ʳƷ��̬�IJ�Ʒ��Ӧ��ʾ��������������ƫ��ָ�꣬��Ӧ����JJF 1070�涨��
�ġ���Ʒ����
���ݷۼ���ʳƷ���ԣ���Ʒ����Ϊ���̱���+ͨ����+�ۡ���ԭ�������Ѵ����ۡ��IJ����ظ����ӣ�
����Ϣ��Դ�������г��ල�����ܾ֣���������콡��������Ͷ�ʹ�������˾ ����ʳƷע�Ჿwww.zhuceabc.cn��
 ;��:tianjianhuacheng
;��:tianjianhuacheng


